Hay noches en las que uno no logra dormir, y a la mañana siguiente el cuerpo se siente más que cansado: parece saturado, sin energía, como si algo dentro hubiera dejado de funcionar con normalidad. Esa sensación va más allá del simple agotamiento mental. Es una presión que viene de lo más profundo del organismo. ¿De dónde surge esta necesidad ineludible de dormir? La ciencia aún no había encontrado una explicación física concreta. Hasta ahora.
Un equipo de la Universidad de Oxford ha identificado un mecanismo biológico que vincula la presión de sueño con un desequilibrio energético en las neuronas. La clave estaría en las mitocondrias, las diminutas estructuras celulares encargadas de generar energía. Cuando se ven sobrecargadas, lanzan una señal de alerta que obliga al cuerpo a dormir. Así, dormir no sería solo descansar: sería una medida urgente de protección celular.
Las neuronas que controlan el sueño y su termómetro energético
El estudio, publicado en la revista Nature, se centró en un grupo de neuronas del cerebro de la mosca de la fruta, conocidas como dFBNs. Estas neuronas son responsables de inducir el sueño y, según los autores, actúan como una especie de sensor interno del estado energético de la célula. En palabras del artículo: “cuando la fuga se vuelve demasiado grande, estas células actúan como disyuntores, activando el sistema hacia el sueño para evitar una sobrecarga”.
Para entender esto, hay que saber que las mitocondrias generan energía a través de una cadena de transporte de electrones. Si hay más electrones de los que pueden ser procesados eficientemente, estos comienzan a “fugarse”, generando moléculas inestables y peligrosas llamadas especies reactivas de oxígeno. Esta fuga no solo es un signo de estrés mitocondrial: es la chispa que activa el mecanismo del sueño.
Dormir para evitar el daño interno
El hallazgo clave es que estas neuronas detectan el exceso de electrones y responden induciendo sueño. Se trata de una respuesta directa, no de una consecuencia indirecta. Así lo expresan los autores en el artículo: “un excedente de electrones mitocondriales induce el sueño”. Esta frase resume toda la hipótesis: cuando hay demasiada energía sin usar acumulada en las mitocondrias, el cuerpo activa el sueño para protegerse.
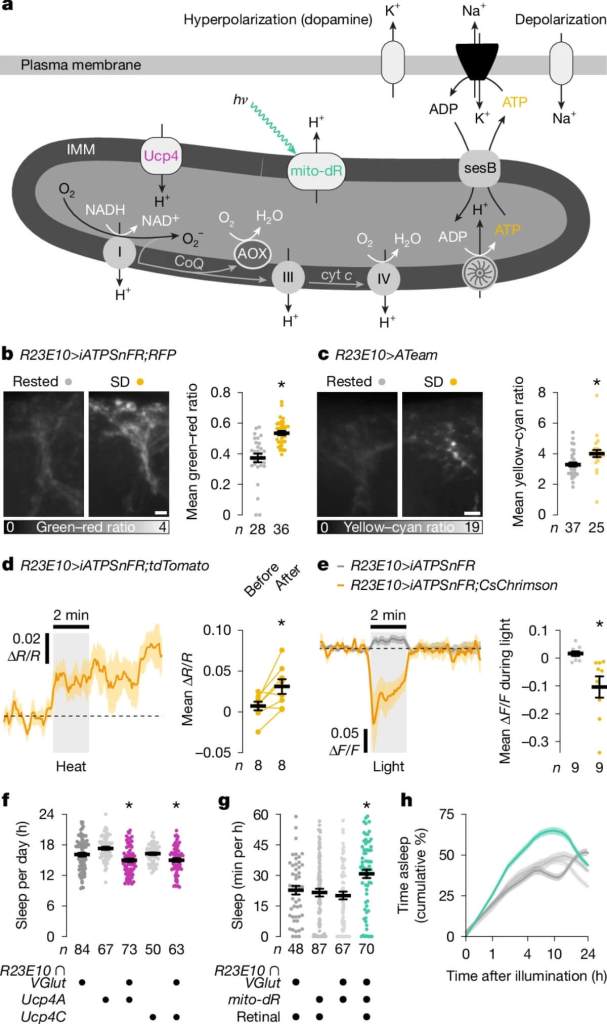
Durante los experimentos, las moscas privadas de sueño mostraban un aumento claro en la producción de energía mitocondrial y cambios en la estructura de estas organelas. Las mitocondrias se hacían más pequeñas, redondeadas y fragmentadas. También se incrementaban los contactos con el retículo endoplasmático y se activaban procesos de limpieza celular. Todo esto indicaba que el cuerpo intentaba frenar una sobrecarga antes de que se produjeran daños mayores.

La paradoja de la vigilia: más energía, más necesidad de dormir
Uno de los aspectos más interesantes del estudio es que el exceso de energía se produce precisamente cuando el cerebro está despierto y las neuronas están inactivas. Esto ocurre porque las neuronas dFBNs consumen menos energía durante la vigilia. Como resultado, el ATP (la principal molécula energética del cuerpo) se acumula. Esto provoca una disminución de la demanda de electrones y, por tanto, una mayor posibilidad de que estos se filtren y generen radicales libres.
El equipo comprobó esto mediante sensores fluorescentes que medían los niveles de ATP en las neuronas. Tras privar de sueño a las moscas, los niveles de ATP aumentaban significativamente en las dFBNs. En cambio, en otras neuronas sin función reguladora del sueño, no se observaban cambios.

El sueño como limpieza mitocondrial
La acumulación de daño en las mitocondrias activa procesos de reparación como la mitofagia, que permite eliminar las mitocondrias defectuosas. Según los autores, el sueño actúa como una fase de recuperación estructural, en la que las mitocondrias se fusionan de nuevo, aumentan de tamaño y recuperan su forma alargada.
Así lo describe el artículo: “la abundancia de contactos mitocondria-retículo endoplasmático en las dFBNs privadas de sueño [...] podría anticipar la proliferación y fusión de mitocondrias durante el sueño de recuperación”. Esto significa que dormir permite no solo reducir la actividad cerebral, sino restaurar físicamente la maquinaria celular que mantiene esa actividad.
Modificar la forma de las mitocondrias cambia la cantidad de sueño
Para probar que este mecanismo es central en el control del sueño, los investigadores manipularon genéticamente la forma de las mitocondrias. Al forzar su fragmentación en las neuronas dFBNs, las moscas dormían menos. Por el contrario, cuando se promovía la fusión mitocondrial, los animales dormían más y con mayor intensidad.
Estas manipulaciones también modificaban las señales eléctricas de las neuronas. Las células con mitocondrias fusionadas mostraban una mayor frecuencia de disparo, lo que se asocia con la inducción del sueño. De nuevo, el sueño aparecía no como una opción, sino como una respuesta celular obligatoria a un desequilibrio interno.
Una explicación para la fatiga en enfermedades mitocondriales
Uno de los aspectos más interesantes de esta hipótesis es que ayuda a entender por qué algunas personas con enfermedades mitocondriales experimentan una fatiga extrema, incluso sin esfuerzo físico. Según el estudio, este agotamiento podría deberse a que sus células tienen una mayor dificultad para gestionar el flujo de electrones, lo que provocaría una presión constante para dormir.
Así lo sugieren los autores: “una sensación abrumadora de cansancio (que no se relaciona con la fatiga muscular) es, de hecho, un síntoma común en las enfermedades mitocondriales humanas”.
¿Y en los mamíferos?
Aunque los experimentos se realizaron en moscas, los autores recuerdan que el vínculo entre metabolismo, consumo de oxígeno y sueño también se observa en otros animales. De hecho, existe una relación entre el tamaño del cuerpo, el consumo de oxígeno por gramo y la duración del sueño: los animales más pequeños, que consumen más oxígeno proporcionalmente, duermen más y viven menos.
El artículo sugiere que esto podría deberse a que sus mitocondrias trabajan con mayor intensidad, generando más radicales libres que deben neutralizarse con más horas de sueño. Así, la necesidad de dormir no sería solo una cuestión de tamaño cerebral o complejidad neuronal, sino una consecuencia directa del mecanismo con el que las células obtienen energía.
Una nueva mirada sobre por qué dormimos
El estudio no niega que el sueño tenga funciones cognitivas, como la consolidación de la memoria o el equilibrio sináptico. Pero plantea que hay un nivel más básico y más antiguo: el sueño como necesidad química, como restauración bioenergética. Dormimos porque nuestras mitocondrias, al trabajar, se desgastan. Y ese desgaste solo puede corregirse desconectando.
Los autores lo resumen así: “la respuesta parece estar escrita en la forma misma en que nuestras células convierten el oxígeno en energía”. Esta frase, sencilla pero contundente, cambia radicalmente el modo en que entendemos el sueño. No es solo una pausa, ni una función del sistema nervioso: es una exigencia del metabolismo celular.
Referencias
- Raffaele Sarnataro, Cecilia D. Velasco, Nicholas Monaco, Anissa Kempf y Gero Miesenböck. Mitochondrial origins of the pressure to sleep. Nature (2025). DOI: https://doi.org/10.1038/s41586-025-09261-y.




