Cuando alguien se resbala en una acera helada, no suele preguntarse por qué el hielo es tan traicionero. Se busca el equilibrio, se lanzan maldiciones al suelo y se aprieta el paso. Lo curioso es que, incluso tras siglos de ciencia, la explicación que nos enseñaron en la escuela sobre ese desliz sigue repitiéndose: el hielo se derrite por la presión o por el calor generado al pisarlo, y esa delgada película de agua es la que nos hace patinar. ¿De verdad esta es la explicación?
No está tan claro. Esa vieja idea acaba de ser desmontada. Un nuevo estudio liderado por el físico Martin Müser y publicado en Physical Review Letters demuestra que ni la presión ni la fricción son los verdaderos culpables de la peligrosidad del hielo. En su lugar, lo que hace que resbalemos tiene que ver con la interacción eléctrica entre moléculas. Se trata de una explicación elegante, basada en simulaciones moleculares, que revoluciona lo que se sabía sobre cómo se comporta el hielo al contacto.
El viejo paradigma que por fin se rompe
Durante casi dos siglos, la teoría dominante sostenía que la fricción al caminar o el peso del cuerpo al pisar el hielo generaban calor suficiente para fundir una finísima capa superficial. Esa agua actuaba como lubricante natural, reduciendo el roce y facilitando el deslizamiento. La hipótesis venía respaldada por nombres ilustres, como James Thompson, hermano de Lord Kelvin.
Pero el nuevo estudio, desarrollado por investigadores de la Universidad del Sarre, ha demostrado que esta explicación es científicamente insostenible. Utilizando simulaciones a nivel molecular, el equipo descubrió que el hielo puede volverse resbaladizo sin necesidad de calor ni de presión extrema, desafiando así el núcleo de la teoría clásica.
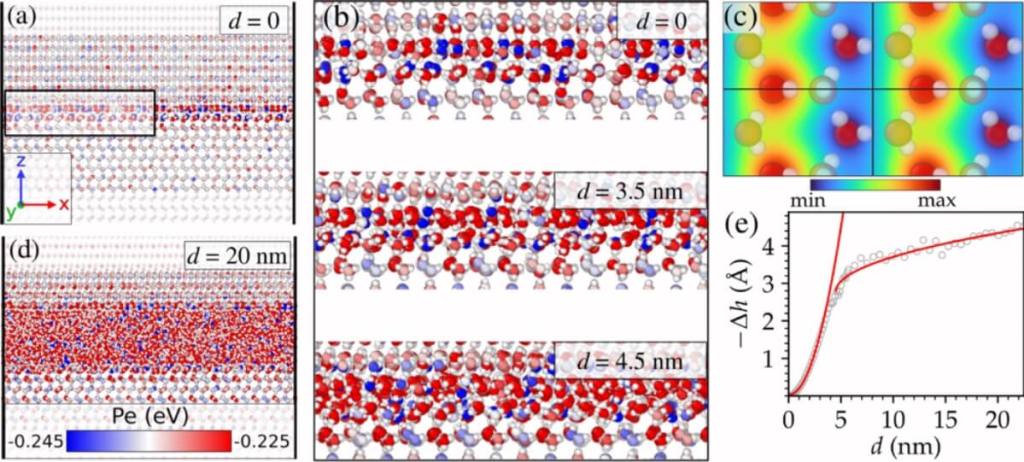
Según el artículo, "las superficies de hielo se licuan sin fundirse termodinámicamente, sino predominantemente mediante una amorfización fría inducida por desplazamiento". Esto implica que la estructura del hielo se desordena localmente cuando entra en contacto con otro material, como una suela de zapato, debido a la interacción entre las cargas eléctricas de ambas superficies.
Dipolos, desorden y superficies que se deforman sin derretirse
Para entender este fenómeno, es esencial saber qué es un dipolo molecular. Se trata de una molécula que tiene una distribución desigual de carga, es decir, un extremo ligeramente positivo y otro ligeramente negativo. En el caso del agua congelada, los dipolos de las moléculas están ordenados de forma estable en una red cristalina.
Cuando otro material, como un zapato o un esquí, entra en contacto con esa superficie, los dipolos del hielo y del objeto interactúan. Esto produce una ruptura del orden, provocando que las moléculas se desorganicen y pasen a un estado amorfo. No es hielo sólido, pero tampoco es agua líquida en el sentido convencional. Es un estado intermedio que se comporta como una capa lubricante ultrafina.
El equipo lo explica así: "La interfaz de hielo-hielo más suave posible, incommensurable, forma sitios fríos soldados localmente, donde el desplazamiento lateral desencadena una amorfización sin calor ni grandes presiones normales". Esta amorfización —es decir, la pérdida del orden cristalino— ocurre sin necesidad de que el hielo alcance su punto de fusión.
¿Qué es la amorfización?
Amorfización es el proceso por el cual un material pierde su estructura cristalina ordenada y se convierte en una forma desorganizada, conocida como estado amorfo. En el caso del hielo, esto significa que las moléculas de agua dejan de estar alineadas de forma regular, como en un cristal, y pasan a un estado caótico, sin patrón definido. Esta transformación no implica que el hielo se derrita en agua líquida, sino que adopta una forma intermedia que actúa como una capa lubricante en la superficie.

El mito de que no se puede esquiar a -40 °C
Una de las creencias más arraigadas, incluso entre esquiadores profesionales, es que por debajo de los -40 °C no se puede esquiar porque no se forma la capa de agua necesaria para deslizarse. Este trabajo demuestra que eso también es incorrecto. Aunque en esas condiciones extremas la capa líquida es más viscosa —“más espesa que la miel”, como la describen los autores en su nota divulgativa—, sigue existiendo.
Lo relevante es que esta fina película no proviene del derretimiento, sino del desorden estructural inducido por el movimiento. Incluso a temperaturas cercanas al cero absoluto, las interacciones dipolares siguen activas y la capa lubricante se forma de todos modos.
Este hallazgo cambia el enfoque para entender el deslizamiento sobre hielo en condiciones extremas. No se trata de cuánta agua se genera al calentar, sino de cómo se reorganizan las moléculas del hielo cuando se aplica una fuerza, por leve que sea.
El rol del material en contacto: no todo resbala igual
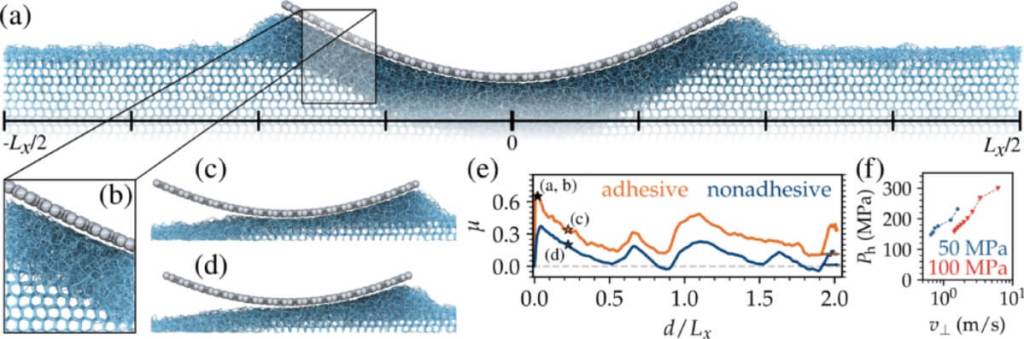
Otro hallazgo importante del estudio es que el tipo de material que entra en contacto con el hielo influye notablemente en el nivel de fricción. Las simulaciones mostraron que las superficies hidrofóbicas —aquellas que repelen el agua— generan menos fricción que las hidrofílicas.
Esto ocurre porque la estructura del agua amorfa se altera menos cuando está en contacto con materiales que no la atraen. Como resultado, la capa lubricante se mantiene estable durante más tiempo, lo que favorece un deslizamiento más eficiente. En palabras de los autores: "Además del agua interfacial, las contrapartes deben ser lisas e hidrofóbicas para que el hielo tenga coeficientes de fricción muy bajos".
Este descubrimiento tiene aplicaciones directas en el diseño de neumáticos, calzado antideslizante y equipos deportivos. Si se puede manipular la fricción a través del material, es posible desarrollar tecnologías que reduzcan significativamente el riesgo de caídas o aumenten el rendimiento en el deporte.
No es calor, es desplazamiento
Quizás uno de los aspectos más contraintuitivos de este trabajo es que el hielo se vuelve más resbaladizo cuanto más frío está. A -10 °C, por ejemplo, el hielo amorfizado presenta mayor viscosidad que a temperaturas más bajas. Pero eso no significa que haya más fricción. De hecho, la tasa de amorfización —el proceso que genera esa capa resbaladiza— es mayor cuando el hielo está más frío.
Esto contradice directamente la idea de que el calor es necesario para fundir el hielo y facilitar el deslizamiento. El estudio compara el comportamiento del hielo a -10 °C y a 10 K (unos -263 °C), y encuentra que "los cristales de hielo más fríos se amorfizan más rápido".
La explicación está en la mecánica molecular. A esas temperaturas, las moléculas están tan rígidas que, al aplicarse una fuerza, no tienen tiempo de reorganizarse y simplemente se desordenan, formando esa capa que permite deslizarse.
Una revolución silenciosa con aplicaciones muy concretas
Aunque este descubrimiento pueda parecer teórico, tiene implicaciones directas en muchos ámbitos de la vida cotidiana y la tecnología. Desde el diseño de neumáticos para carreteras heladas hasta la fabricación de esquís o el desarrollo de materiales antifricción, entender el verdadero mecanismo del deslizamiento sobre hielo permite tomar decisiones basadas en física real, no en suposiciones heredadas del siglo XIX.
También invita a revisar cómo se enseña la física del hielo en los niveles educativos básicos. La nueva evidencia muestra que el fenómeno no depende principalmente del calor o la presión, sino de efectos estructurales y eléctricos a nivel microscópico, que pueden modelarse con herramientas modernas de simulación.
Por último, este avance demuestra el valor de la ciencia básica. Lo que comenzó como una curiosidad sobre por qué el hielo es resbaladizo ha terminado cambiando nuestra comprensión de un fenómeno cotidiano. Y lo ha hecho con una herramienta invisible pero poderosa: la simulación por ordenador a nivel atómico.
Referencias
- Achraf Atila, Sergey V. Sukhomlinov, Martin H. Müser. Cold Self-Lubrication of Sliding Ice. Physical Review Letters. DOI: 10.1103/1plj-7p4z.




