Los primeros achaques no siempre llegan como uno los espera. A veces es una rodilla que ya no responde igual, otras veces es un cansancio que antes no estaba o una cicatriz que tarda más en desaparecer. No se trata de alarmismo ni de quejas propias de quien cruza la barrera de los 30: hay algo que cambia dentro del cuerpo, aunque por fuera todo parezca seguir igual. Pero ¿a qué ritmo envejecen realmente nuestros órganos? ¿Y ese ritmo es el mismo para todos? Un nuevo estudio ha trazado el primer mapa proteómico integral del envejecimiento humano en 13 órganos diferentes y sus hallazgos son tan reveladores como inquietantes.
Publicado en la revista Cell en 2025, el trabajo liderado por la Academia China de Ciencias ha construido una especie de “reloj molecular” basado en proteínas, que permite estimar la edad biológica de distintos tejidos. Usando muestras de 76 individuos entre los 14 y los 68 años, los científicos observaron patrones únicos de envejecimiento en cada órgano. Lo más sorprendente es que este deterioro no empieza con la vejez, ni siquiera en la madurez tardía: muchos cambios se activan en plena adultez temprana, marcando un punto de inflexión antes de los 50. Los autores afirman que “los relojes proteómicos mostraron inflexiones consistentes en la mediana edad, entre los 45 y 55 años”.
Un atlas proteómico del envejecimiento
Este estudio representa la primera caracterización a gran escala del envejecimiento a nivel proteico en múltiples tejidos humanos. Más de 12.700 proteínas fueron cuantificadas en órganos del sistema cardiovascular, digestivo, inmunológico, endocrino, respiratorio, musculoesquelético y tegumentario. En total, se analizaron 516 muestras de tejido y plasma con espectrometría de masas de alta resolución y análisis transcriptómico paralelo.
Una de las claves del trabajo es la observación del desacoplamiento entre el transcriptoma (ARN mensajero) y el proteoma (proteínas realmente producidas), lo que refleja una pérdida progresiva de control en la síntesis de proteínas. Esta desconexión fue especialmente marcada en el bazo, los ganglios linfáticos y el músculo. Como afirman los investigadores, se detectó una “pérdida asociada a la edad de la correlación ARN-proteína en todos los tejidos”. Esto implica que, con el paso de los años, aunque los genes aún "den la orden", el cuerpo tiene cada vez más dificultades para fabricar las proteínas adecuadas en el momento justo.
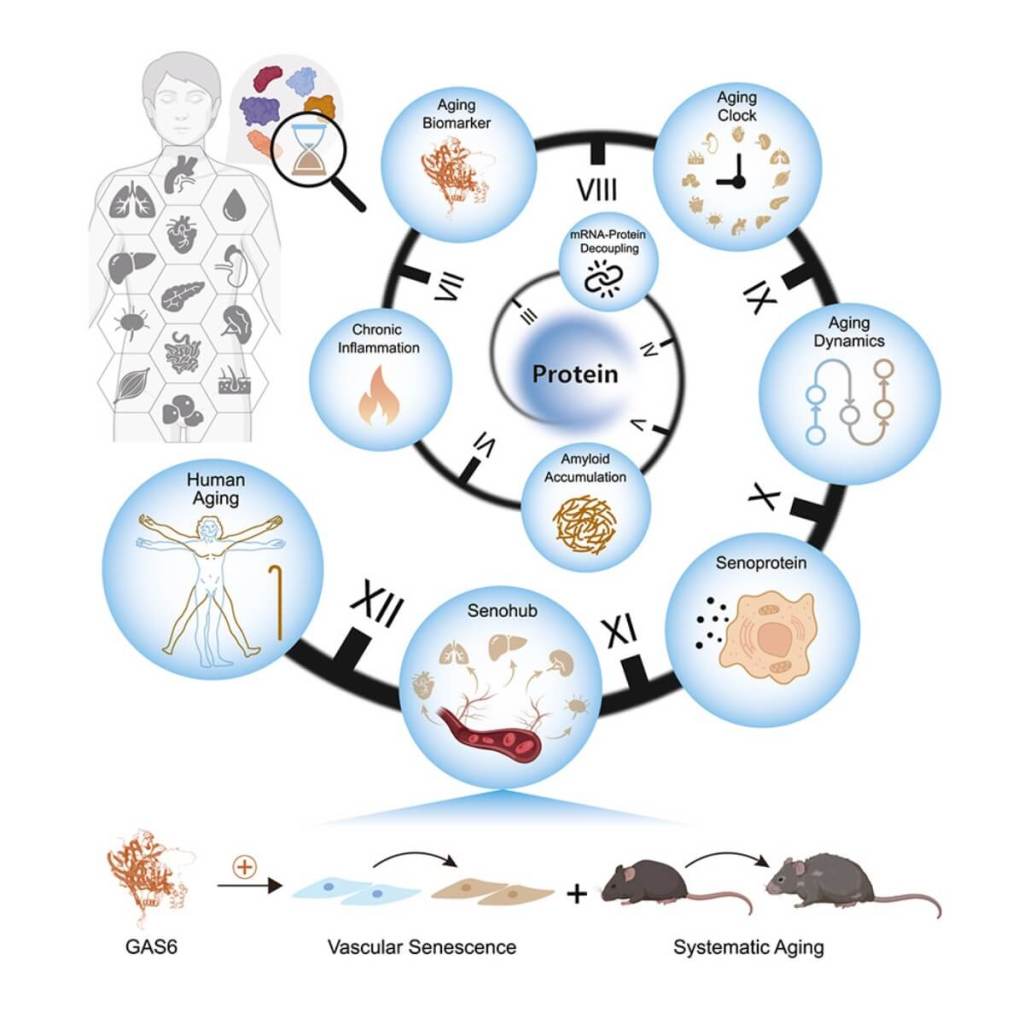
El eje inflamatorio del envejecimiento
Uno de los descubrimientos más notables del estudio es el papel central de ciertas proteínas relacionadas con la inflamación y la inmunidad. Se identificó un eje formado por proteínas amiloides, inmunoglobulinas y factores del complemento, que se acumulan en los tejidos envejecidos. Este “eje amiloide-inmunoglobulina-complemento”, como lo llaman los autores, representa un bucle de retroalimentación entre proteínas mal plegadas, activación inmunitaria y daño tisular crónico.
Entre las proteínas más destacadas está SAP (componente P del amiloide sérico), cuya presencia aumentó en al menos seis tejidos. El SAP no solo se acumuló de forma observable mediante análisis histológico, sino que además indujo senescencia e inflamación en células endoteliales humanas. Esto sugiere que no se trata de un simple marcador pasivo del envejecimiento, sino de un actor activo en el deterioro funcional del organismo.

Los relojes del cuerpo: cada órgano a su ritmo
Uno de los avances más útiles de este trabajo es la construcción de “relojes proteómicos” específicos para cada órgano. Mediante regresión con redes elásticas (elastic net), los investigadores pudieron predecir la edad biológica de tejidos individuales con una alta precisión (correlaciones de Spearman entre 0.74 y 0.95). Estas herramientas son capaces de detectar cuándo un órgano empieza a envejecer más rápido que los demás.
Por ejemplo, la aorta mostró los cambios más sostenidos a lo largo del tiempo. También se observó una proteína —TIMP3— repetida en nueve de estos relojes, lo que sugiere que puede ser un regulador común del envejecimiento multiorgánico. En conjunto, los datos permiten afirmar que el envejecimiento no es uniforme: “cada órgano parece tener su propia trayectoria temporal de deterioro”.
Proteínas que propagan el envejecimiento
Uno de los hallazgos más intrigantes es la identificación de lo que los autores llaman un “senohub”: órganos que no solo sufren el envejecimiento, sino que también lo propagan a otros tejidos a través de proteínas secretadas. El principal de estos “emisores” sería la aorta, que a través de proteínas como GAS6 activa receptores en células del sistema inmune y vascular, acelerando la senescencia a nivel sistémico.
La proteína GAS6, en particular, aumentó con la edad tanto en plasma como en tejido aórtico. En células humanas, indujo marcadores de senescencia, elevó IL-6 (una molécula proinflamatoria) y redujo la capacidad de formación de vasos nuevos. En ratones de mediana edad, las inyecciones de GAS6 provocaron disfunción vascular, inflamación tisular y deterioro físico observable.
Estas observaciones indican que ciertas proteínas no solo reflejan el envejecimiento, sino que también lo inducen. Un fenómeno similar se observó con GPNMB, otra proteína cuya administración en ratones provocó inflamación vascular y pérdida de movilidad. El estudio concluye que “los tejidos vasculares actúan tanto como sensores como transmisores de señales de envejecimiento”.
Del laboratorio a la salud pública
Más allá de su valor como investigación básica, este mapa proteómico ofrece herramientas con gran potencial clínico. Los relojes proteómicos podrían usarse para evaluar la edad biológica de pacientes de forma personalizada, detectando envejecimiento prematuro en órganos específicos. Esto permitiría intervenciones más tempranas y dirigidas, como terapias antiinflamatorias o cambios de estilo de vida focalizados.
Además, el estudio señala que algunos cambios comienzan antes de lo que se pensaba. Entre los 30 y 45 años ya se activan varias trayectorias de deterioro, especialmente en tejidos vasculares y glandulares como la aorta y las glándulas suprarrenales. Esto plantea una pregunta importante para la salud pública: ¿deberíamos comenzar a vigilar y prevenir el envejecimiento sistémico desde la juventud?
A medida que avancen las tecnologías de análisis proteómico y se sumen nuevas cohortes más amplias y diversas, el mapa del envejecimiento humano podrá completarse con mayor resolución. De momento, este estudio representa un punto de inflexión: por primera vez, se ha trazado cómo envejece cada órgano, con una claridad que acerca la biología a la práctica clínica.
Referencias
- Yingjie Ding et al. Comprehensive human proteome profiles across a 50-year lifespan reveal aging trajectories and signatures. Cell (2025). DOI: 10.1016/j.cell.2025.06.047.