Todos los días, la nariz permite detectar aromas, desde el café recién hecho hasta la lluvia sobre la tierra seca. Pero lo que pocas personas saben es que las neuronas responsables del olfato no son permanentes. Se reemplazan con frecuencia a lo largo de la vida. Esta regeneración constante es una rareza dentro del sistema nervioso. Esta es la razón por la que ha sido durante años un enigma para la biología.
Un nuevo estudio acaba de arrojar luz sobre este fenómeno. Publicado en Stem Cell Reports, el trabajo revela cómo las células madre en la nariz se organizan y transforman en neuronas especializadas. Gracias a experimentos con embriones de pez cebra, imágenes de alta resolución y modelado computacional, el equipo identificó un mecanismo que permite que el sistema olfativo se renueve de forma eficiente y continua.
Las neuronas del olfato: una excepción que pide explicación
A diferencia de muchas regiones del cerebro, el epitelio olfativo tiene una sorprendente capacidad para fabricar nuevas neuronas de forma regular. En los seres humanos, este proceso ocurre incluso en la edad adulta, permitiendo que el olfato se mantenga a pesar del desgaste natural o ciertas lesiones.
Pero este fenómeno no es tan simple como reemplazar piezas gastadas. Para que funcione, las células madre deben decidir en qué tipo celular convertirse, coordinarse con otras, migrar a su sitio correcto y hacerlo en medio de señales ruidosas y variables. La pregunta que se plantearon los autores fue clara: ¿cómo se organiza este proceso tan complejo en un entorno tan dinámico?
Un vecindario celular con reglas claras
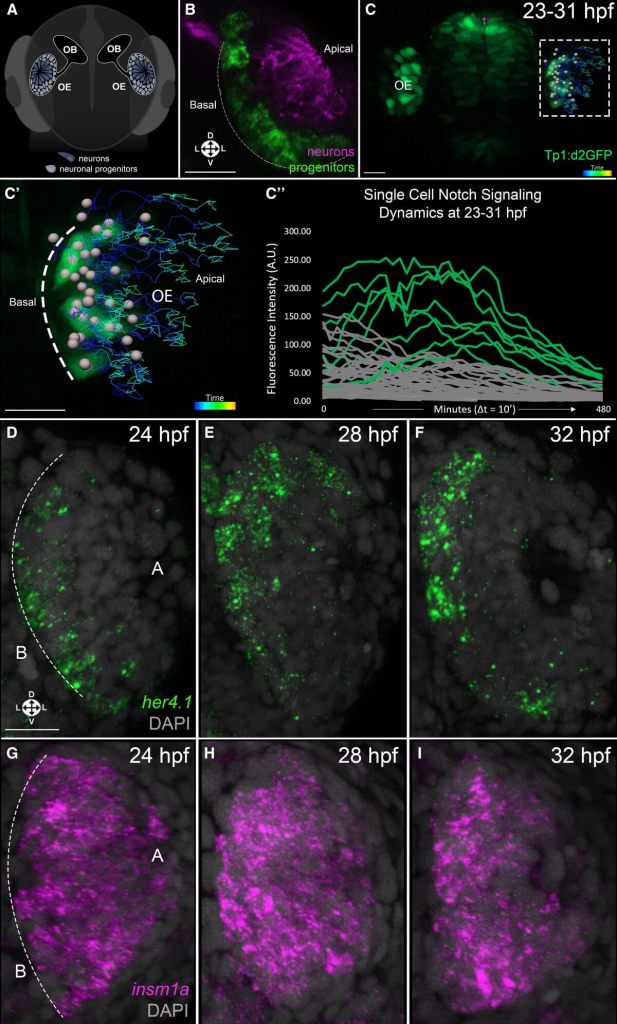
El estudio demostró que la clave está en la formación de “vecindarios celulares”: agrupaciones transitorias de progenitores que actúan como nichos especializados. En cada vecindario hay un centro celular con alta actividad de la vía de señalización Notch y células vecinas con alta expresión del gen insm1a, que promueve la diferenciación neuronal.
Este patrón no es aleatorio. Como afirman los autores, “las células progenitoras se agrupan en vecindarios neurogénicos que actúan como nichos transitorios para generar nuevas neuronas olfativas”. Estos grupos permiten que las señales entre células —que pueden ser ruidosas o poco claras— se transformen en decisiones precisas: seguir siendo progenitoras o diferenciarse en neuronas.
Por otra parte, se observó que las neuronas recién nacidas migran hacia la superficie del epitelio, donde se integran en la estructura sensorial llamada roseta olfativa.
Notch vs. Insm1a: una rivalidad que define el destino celular
Uno de los hallazgos más interesantes del estudio fue el descubrimiento de un interruptor genético de tipo bistable, formado por la interacción entre la vía Notch y el gen insm1a. Estas dos señales se inhiben mutuamente: cuando una está activa, la otra se apaga. Esto crea un sistema que fija el destino de las células progenitoras de forma estable.
Los investigadores lo describen así: “la neurogénesis está impulsada por el antagonismo mutuo entre la señalización Notch y insm1a, que responde a señales de ácido retinoico provenientes de otros órganos”. Es decir, la decisión sobre el destino celular no solo depende de lo que pasa en la nariz, sino también de señales que llegan desde otros lugares, como los ojos.
Este mecanismo de alternancia permite que el sistema responda de forma flexible a los cambios, pero al mismo tiempo, asegura resultados consistentes.

Un empujón desde el ojo: la señal que activa el proceso
Otra pieza clave del rompecabezas es el ácido retinoico (RA), una molécula derivada de la vitamina A. En este estudio, se comprobó que el RA no se produce en la nariz, sino en el ojo en desarrollo. Desde allí, viaja hasta el epitelio olfativo para modular el equilibrio entre Notch e insm1a.
Los autores demostraron que al reducir la producción de RA, se frena el proceso de diferenciación neuronal. Esto sugiere que existe un diálogo interorgánico, donde el ojo actúa como una especie de regulador del olfato durante el desarrollo. La expresión espacial de enzimas que metabolizan el RA también ayuda a delimitar las zonas donde se generan neuronas.
Este hallazgo refuerza la idea de que los órganos en desarrollo no actúan de forma aislada, sino que intercambian señales constantemente para coordinar su maduración.
Movimiento con destino: cómo las neuronas migran a su lugar final
Una vez que se han diferenciado, las nuevas neuronas no se quedan donde nacieron. Se desplazan desde la base del epitelio hacia la parte superior, donde se integran en el tejido sensorial. Este movimiento está guiado por una señal producida por otras neuronas ya maduras: una proteína llamada BDNF.
La investigación comprobó que el BDNF actúa como una señal de atracción, y que las neuronas en formación responden a ella a través de un receptor llamado TrkB. Cuando este sistema se bloquea, las células siguen moviéndose, pero pierden la dirección correcta.
Este mecanismo asegura que las nuevas neuronas lleguen exactamente donde se necesitan, manteniendo el orden del sistema sensorial. También revela que incluso las neuronas recién nacidas reciben instrucciones de las que ya están establecidas.
Lo pequeño también cuenta: un modelo para entender sistemas complejos
Uno de los grandes aportes del estudio es su enfoque multiescala. A través de imágenes en vivo, secuenciación de ARN y modelos computacionales, se logró capturar cómo decisiones a nivel molecular se traducen en patrones celulares organizados.
El modelo matemático desarrollado permite explicar cómo una red genética con variaciones estocásticas puede generar resultados estables, gracias al interruptor bistable. Este tipo de análisis ayuda a comprender no solo el desarrollo del sistema olfativo, sino también procesos similares en otros órganos.
Como resumen el artículo, “nuestros hallazgos revelan cómo redes de señalización estocásticas regulan espacial y temporalmente el equilibrio entre progenitores y derivados”, manteniendo la neurogénesis en un sistema sensorial tan complejo como la nariz.
Lo que nos dice el olfato sobre el cerebro
Aunque el estudio se centra en el epitelio olfativo del pez cebra, sus implicaciones van más allá. El olfato es uno de los pocos sentidos que sigue renovando sus neuronas durante toda la vida, incluso en humanos. Comprender cómo lo logra podría abrir caminos para terapias regenerativas en otras regiones del cerebro.
Además, este trabajo ofrece un modelo de cómo células individuales cooperan como grupo para tomar decisiones colectivas, algo que podría aplicarse a otros tejidos y sistemas. Desde el desarrollo embrionario hasta la regeneración de tejidos dañados, los mecanismos descubiertos podrían tener un papel importante.
En un momento en que se busca entender mejor la plasticidad del cerebro, este hallazgo huele a avance importante.
Referencias
- Sriivatsan G. Rajan, Lynne M. Nacke, Joseph N. Lombardo, Farid Manuchehrfar, Kaelan Wong, Pinal Kanabar, Elizabeth A. Somodji, Jocelyn Garcia, Mark Maienschein-Cline, Jie Liang, Ankur Saxena. Progenitor neighborhoods function as transient niches to sustain olfactory neurogenesis. Stem Cell Reports. https://doi.org/10.1016/j.stemcr.2025.102575.